发布时间:2021-11-11 13:55:28
国家药监局药审中心发布《中国新药注册临床试验现状年度报告(2020年)》

为全面掌握中国新药注册临床试验进展,加强药品监管能力建设,药审中心根据药物临床试验登记与信息公示平台登记信息,首次对中国新药注册临床试验现状进行了全面汇总分析,撰写形成《中国新药注册临床试验现状年度报告(2020年)》。
本报告根据2020年度登记的药物临床试验信息,从申办者类型、药物类型、试验品种、适应症、试验分期、特殊人群试验、临床试验的组长单位、启动耗时和完成情况等角度对临床试验的整体进展、主要特点、变化趋势、和突出问题等进行汇总、梳理和分析。
后续药审中心将按年度报告新药注册临床试验情况,以中国新药注册临床试验登记数据为依托,聚焦监管创新,提高监管效能,在推动药品监管能力现代化中加强与业界沟通交流,增加信息透明度,助推中国新药临床试验高质量健康发展。
附件:《中国新药注册临床试验现状年度报告(2020年)》
国家药品监督管理局药品审评中心
2021年11月10日
附件
《药物警戒体系主文件撰写指南(征求意见稿)》








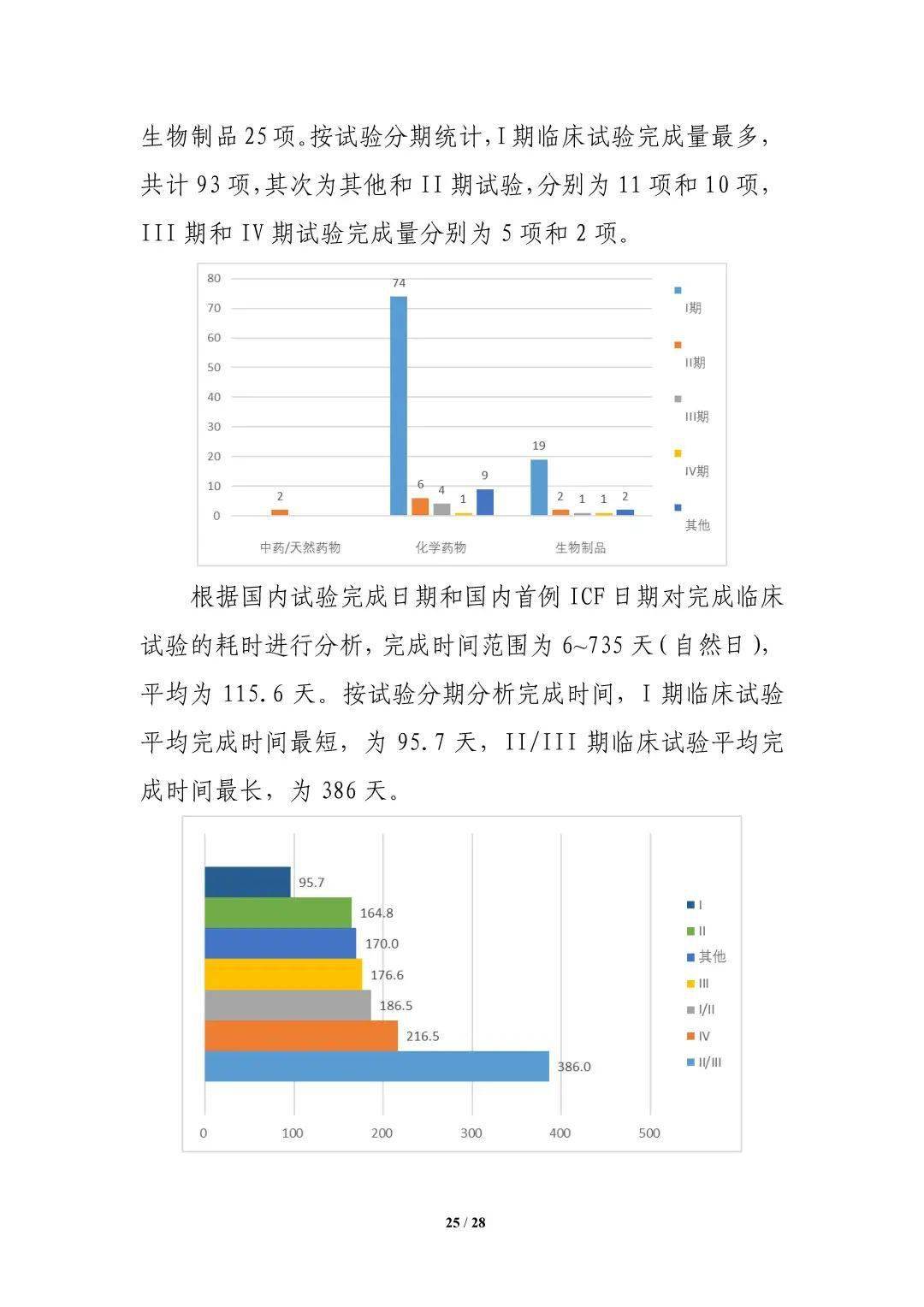
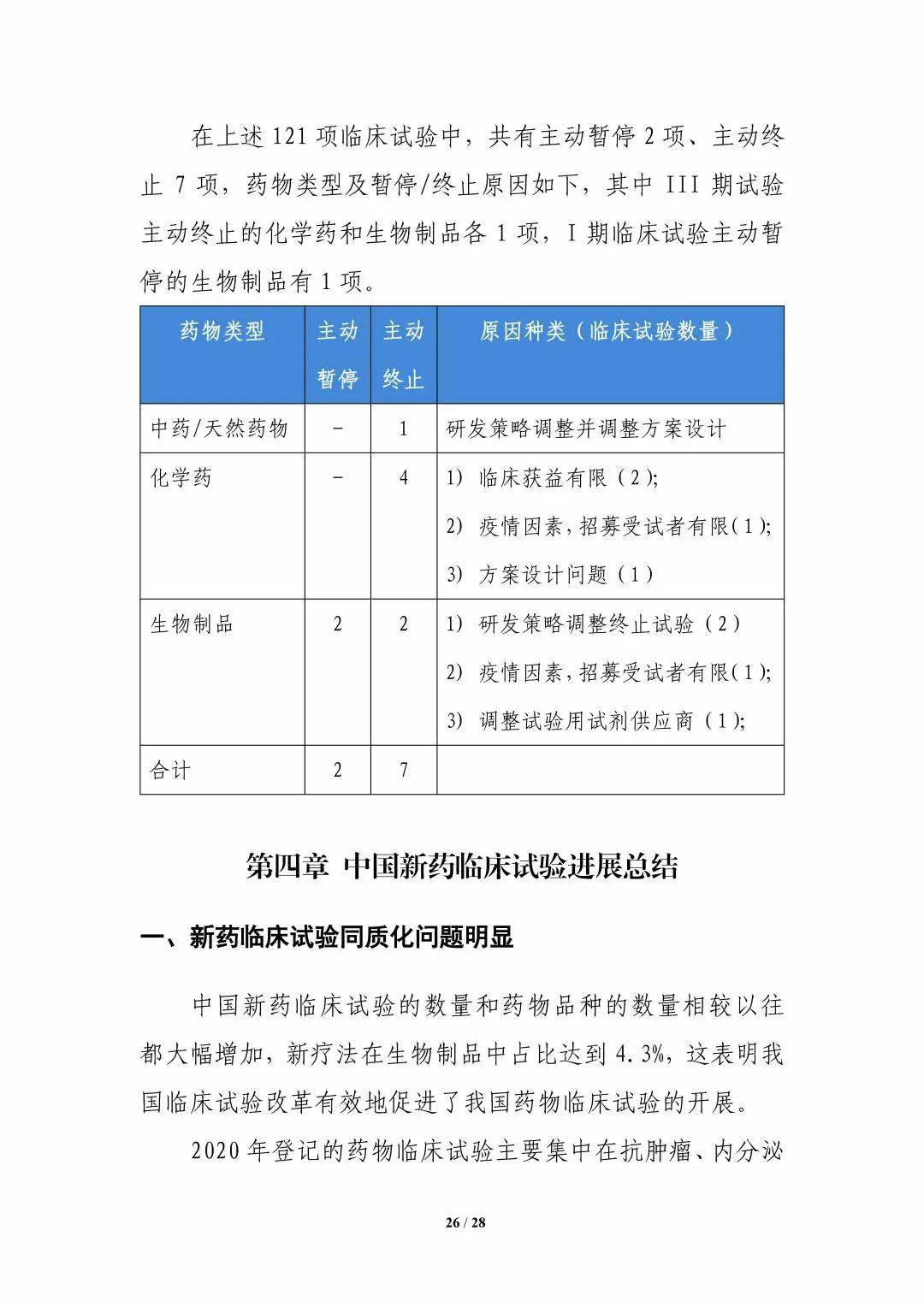


来源:国家药品监督管理局药品审评中心 官网 2021年11月10日